Continua il racconto del Punto d’Ascolto organizzato dalla Fondazione Malattie Miotoniche il 15 dicembre scorso.
Il prof. Meola interviene con un focus sui trial in corso, dettagliando lo stato avanzamento lavori per ciascun progetto delle case farmaceutiche impegnate nella ricerca sulla distrofia miotonica.
 Per comprendere bene i trial e cosa stiano producendo in termini di risultati, il prof. Meola ha evidenziato le distinzioni tra DM1 e DM2 da un punto di vista genetico.
Per comprendere bene i trial e cosa stiano producendo in termini di risultati, il prof. Meola ha evidenziato le distinzioni tra DM1 e DM2 da un punto di vista genetico.
La diapositiva presentata descrive: la tipologia di cromosomi e di geni implicati per ciascuna forma, il grado di espansione delle triplette nei rispettivi geni, in base alla quale si definisce il livello di espressione della patologia.
Le due forme sono entrambe autosomiche dominanti, vuol dire che la Distrofia Miotonica è una malattia con una penetranza del 100%, quindi i figli della persona affetta avranno il 50% di possibilità di essere malati di DM.
Inoltre nella DM1 esiste l’anticipazione genetica, vuol dire che, anche se un genitore può essere moderatamente affetto, i figli manifestano, con certezza, una forma di DM più grave.
 Si può parlare di DM1 quando il suo gene, DMPK, presenta un grado di espansione delle triplette superiore a 50.
Si può parlare di DM1 quando il suo gene, DMPK, presenta un grado di espansione delle triplette superiore a 50.
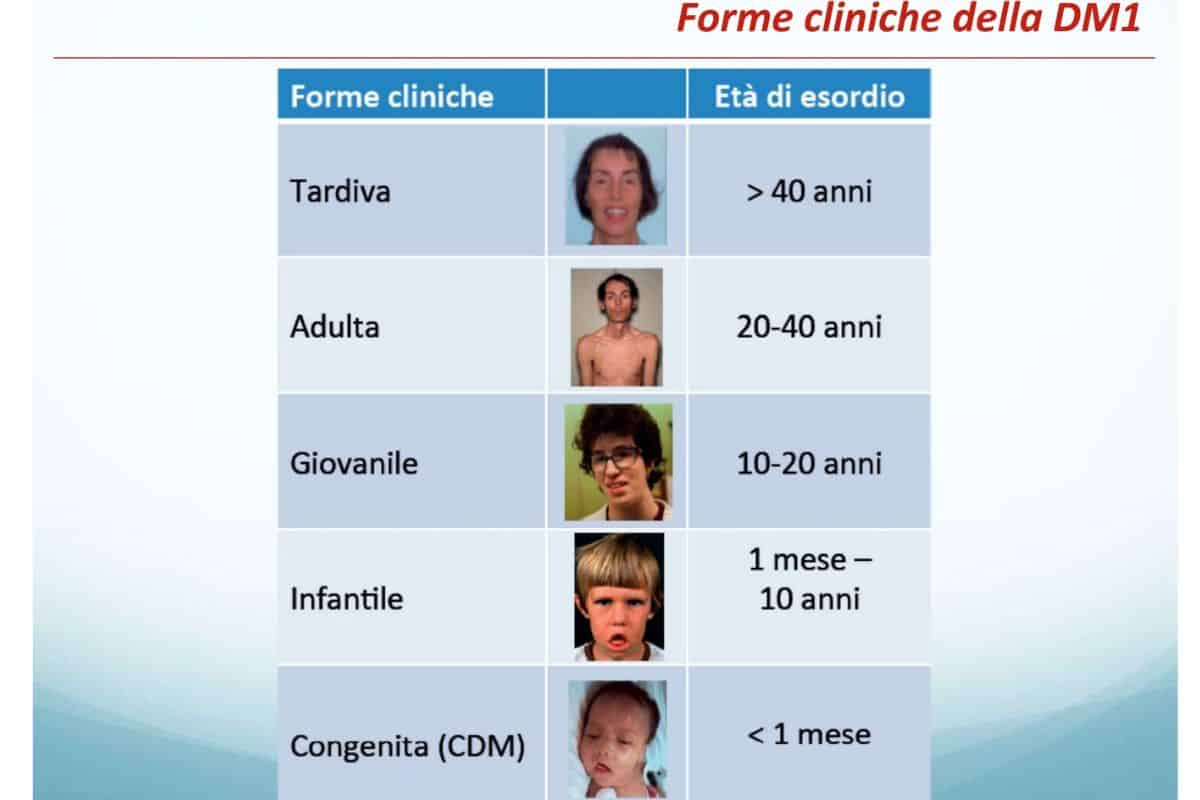
Abbiamo 5 forme cliniche di DM1: congenita (meno di un mese), infantile (1-10 anni), giovanile (10 – 20 anni), adulta (20 – 40 anni) e tardiva (maggiore di 40 anni).
Attraverso la seguente diapositiva, il Prof. Meola sintetizza cosa accade a livello di geni nella persona affetta da Distrofia Miotonica di tipo 1.
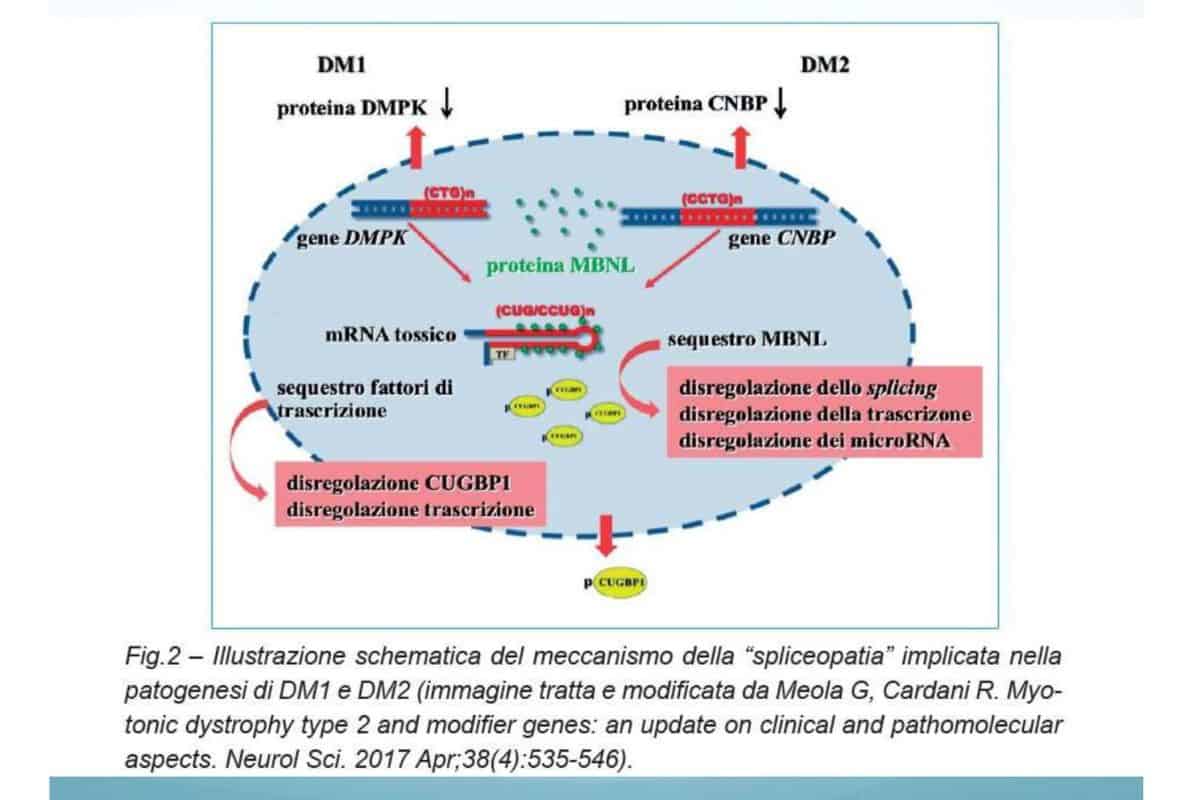 La causa della malattia sta nella copia del gene principale, ovvero l’RNA, che diventa tossico e si accumula in tutte le cellule dell’organismo, sequestrando le proteine, come la MBNL, che svolgono determinate funzioni.
La causa della malattia sta nella copia del gene principale, ovvero l’RNA, che diventa tossico e si accumula in tutte le cellule dell’organismo, sequestrando le proteine, come la MBNL, che svolgono determinate funzioni.
Inficiare le funzioni delle proteine vuol dire avere una serie di problemi diffusi: cardiaci, cognitivi, di sviluppo evolutivo etc…
A settembre 2022 è stata aggiornata la pipeline delle case farmaceutiche impegnate nello studio della distrofia miotonica. I progetti presentano una fase preclinica, durante la quale vengono svolte sperimentazioni sugli animali e le fasi 1 e 2 nelle quali vengono coinvolti i pazienti.
Di seguito un elenco delle case farmaceutiche coinvolte:
Amo Pharma: è impegnata nello studio della distrofia miotonica congenita (CDM). Lo studio è’ in fase clinica e, fino ad oggi, ha dimostrato che il farmaco tideglusib agisce sul RNA tossico. Ciò consente ai bambini affetti di riacquistare maggiore mobilità e presenza cognitiva.
Harmony Biosciences: è impegnata nella valutazione dell’efficacia del farmaco Pitolisant per combattere la sonnolenza diurna, tipica nei pazienti con distrofia miotonica. Lo studio sta dimostrando che tale farmaco aumenta la trasmissione dell’istamina nel cervello e ciò rende più vigile il paziente.
Dyne Therapeutics: sta studiando un meccanismo che riduca l’RNA tossico soprattutto nel muscolo. Hanno creato un composto trivalente, costituito da un anticorpo, un oligonucleotide e un linker, che riesce a penetrare i tessuti muscolari. Lo studio è al momento nella fase preclinica, è prevista una sperimentazione a breve in USA su una coorte di 40-50 pazienti.
PepGen: anche questo studio ha l’obiettivo di ridurre l’RNA tossico ma con un approccio differente. Si utilizza il farmaco, PGN – EDODM1, che favorisce la disponibilità di oligonucleotidi. Studio in fase preclinica, prevista prima sperimentazione sui pazienti nell’arco del 2023.
Arthex Biotec: è l’unica casa farmaceutica europea – spagnola nella fattispecie – impegnata nello studio della DM. Essa studia il comportamento di piccole molecole chiamate MIR che agiscono nell’RNA tossico. I ricercatori hanno somministrato il farmaco, ATX-01 che contiene antiMIR, negli animali conseguendo non solo una riduzione degli accumuli di RNA, ma un mantenimento nel tempo di tale riduzione.
Nel 2023 partirà la sperimentazione su pazienti, affetti da DM1 nella forma adulta, che presentano una spiccata miotonia.
Richiedi copia del libro “Linee guida” per la gestione clinica e presa in carico del paziente DM.
Scarica la presentazione completa dell’intervento.
Video registrazione intervento integrale con inizio al punto 2.12.44.